



设想这样一个场景:一个携带Y染色体的细胞,在不依赖任何胚胎组织的情况下,在培养皿中被引导构建出结构完整的睾丸微环境,并在其中孕育出能够产生健康后代的成熟精子。
这不是科幻情节,而是近期《Science》杂志发表的一项研究展示的真实突破。这项研究首次在体外完整重现了从多能干细胞到功能性睾丸组织、再到成熟精子的全过程。锦欣国际(梦美生命)美国HRC Fertility长期关注生殖医学基础研究,今天带您了解这项可能改写未来生殖医学格局的科学进展。
体细胞决定性别,微环境决定生育
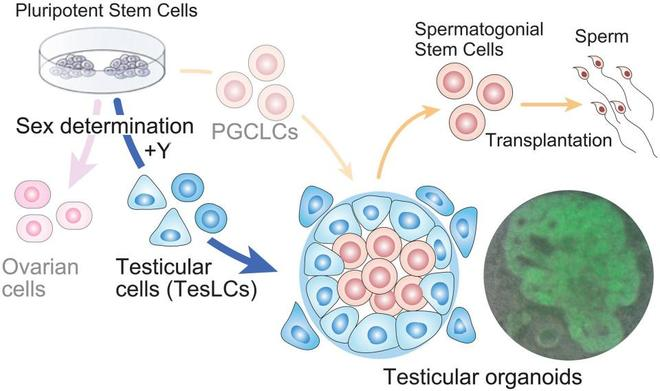
在哺乳动物发育中,性别决定由体细胞主导。胚胎早期,生殖细胞处于未分化状态,真正决定它们命运的,是周围的性腺体细胞。如果这些体细胞被引导分化为支持细胞,就会形成睾丸微环境,促使生殖细胞向精子方向发育;如果分化为颗粒细胞,则形成卵巢微环境。
过去,研究人员已能利用多能干细胞诱导出原始生殖细胞样细胞。但由于缺乏能提供正确信号的体细胞微环境,这些生殖细胞难以继续发育成熟。如何重构睾丸微环境,成为该领域核心挑战[1]。
信号抑制:将细胞导向雄性命运
研究发现,在体外培养条件下,细胞的默认发育路径偏向雌性。即使是XY细胞,若无外界干预,也会向卵巢方向分化。
研究人员在培养基中引入WNT和BMP信号通路抑制剂,成功将细胞命运扳向雄性轨道。实验数据显示,只有XY细胞能在抑制剂作用下转化为表达SOX9的支持细胞,XX细胞则无法跨越性别鸿沟。这些诱导出的细胞被命名为睾丸体细胞样细胞[1]。
人工微环境支持精子发生
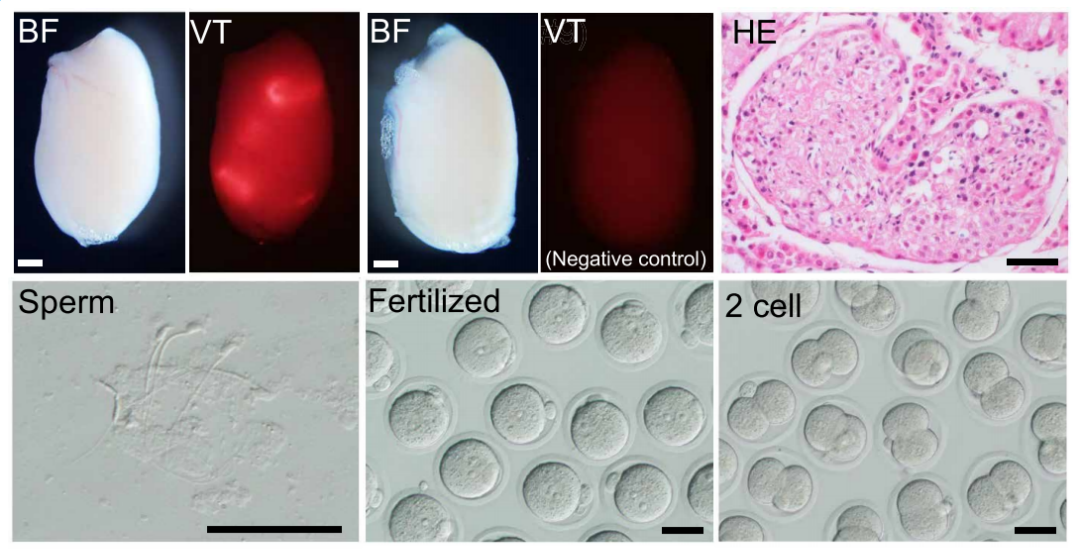
将睾丸体细胞样细胞与原始生殖细胞样细胞共培养后,细胞开始自组织。显微镜下可见支持细胞排列成生精小管样结构,生殖细胞整齐排列于小管内部。间质区域出现睾丸间质细胞,基底膜有层粘连蛋白沉积,标志着一个功能完备的人工睾丸微环境形成。
在这一微环境内,生殖细胞启动分化:部分表达PLZF(精原干细胞标志),部分表达SYCP3(减数分裂标志),表明细胞已进入精子发生程序[1]。

功能验证:健康后代诞生
为验证这些生殖细胞的功能,研究人员将其从类器官中提取并移植到先天性缺乏生精细胞的小鼠睾丸内。10周后,移植细胞在宿主睾丸内扎根并形成生精克隆,从中提取到形态正常的成熟精子。
利用这些精子对卵母细胞实施单精子注射,受精率达93.8%,胚胎移植后25只健康小鼠顺利诞生。基因检测证实,这些幼崽源自培养皿中人工构建的睾丸微环境。幼崽成年后全部展现正常繁育能力[1]。

美国HRC Fertility视角:对生殖医学的潜在意义
这项研究的价值体现在两个层面。一是提供了一个研究平台,使科学家能将不同基因型的生殖细胞与体细胞进行组合,精准分析基因在性别决定和生育中的作用。二是它为未来男性不育治疗描绘了新可能——对于因化疗或性发育异常导致生殖微环境受损的患者,理论上可利用自身干细胞在体外重塑健康睾丸,培育具有繁育能力的精子。
对于辅助生殖领域而言,深入理解生殖细胞与体细胞微环境的相互作用,有助于更准确评估遗传检测结果。胚胎植入前遗传学检测能够在胚胎移植前筛查已知单基因病,其准确性高度依赖于对基因型与表型关联的认知。随着对生殖微环境重建机制的理解不断深入,我们有望更精准地评估遗传变异对生育能力的实际影响,为有遗传病风险的家庭提供更全面的生殖选择。
参考文献:
[1] Takashi Yoshino et al.,Reconstitution of sex determination and the testicular niche using mouse pluripotent stem cells.Science391,eaea0296(2026).
客服咨询:400-111-1951
服务咨询:155-0121-7090
中国地址:北京市丰台区丽泽路24号平安幸福中心
美国办公室:17800 Castleton St, Unit 263, City of Industry, CA United States, 91748

微信扫码添加VIP客服





